新冠肺炎疫苗的開發
計劃主持人 : 黃立民特聘教授/國立臺灣大學醫學院小兒科;張淑媛教授/國立臺灣大學醫學院醫學檢驗暨生物技術學系
單位 :國立臺灣大學防疫科學研究中心
1. 開發以去活化SARS-CoV-2病毒做為疫苗:
已完成病毒基因穩定性測試,並將去活化病毒條件確立,包括去活化後以電顯確認病毒型態的完整性。已開始去活化病毒的免疫反 應。後續會依實驗結果進行病毒攻讀實驗。
2. 開發基於SARS-CoV-2受體結合區(RBD)的疫苗:
已確認所設計的RBD可引發中和抗體的產生,論文已發表。目前在建立follicular dendritic cell (fDC)-targeting antigen vaccine的實 驗測試。
3. 發展使用HBc類病毒顆粒來誘發黏膜性免疫反應的SARS-CoV-2疫苗:
已確認HBc及RBD的重組蛋白表現,在以鼻腔黏膜方式免疫小鼠的實驗結果中顯示,HBc類病毒顆粒及RBD的混和物能有效的誘發 血清中的RBD特異性抗體反應及在肺臟沖洗液中的分泌型IgA反應。
1. 去活化SARS-CoV-2病毒疫苗:
去活化SARS-CoV-2病毒(NTU27)的免疫接種如下。總共10隻C57BL / 6小鼠,包括四隻接受3 µg病毒蛋白加鋁鹽,四隻接受6 µg病毒蛋白加鋁鹽的小鼠和兩隻僅接受鋁鹽作為對照的小鼠。在第0天和第7天進行兩次肌肉注射免疫。結果觀察到針對S蛋白和NP蛋白的RBD的抗體反應升高。
分析了抗原刺激的T細胞(IL6,IL9,IL17,IFN-γ)的免疫細胞譜(CD4+,CD8+,TH1,TH2,TH17細胞)和細胞激素譜。肌內註射佐劑與去活化的COVID-19病毒混合可提高脾臟細胞中CD11b+細胞和嗜中性白血球細胞的比例。去活化的COVID-19免疫會影響小鼠脾臟的細胞組成。與對照組相比,肌內注射佐劑與6μg去活化的COVID-19病毒混合可引起更高的CD4+和CD8+ T細胞IFN-γ反應,而3μg病毒蛋白的組別則可降低T細胞IFN-γ反應。
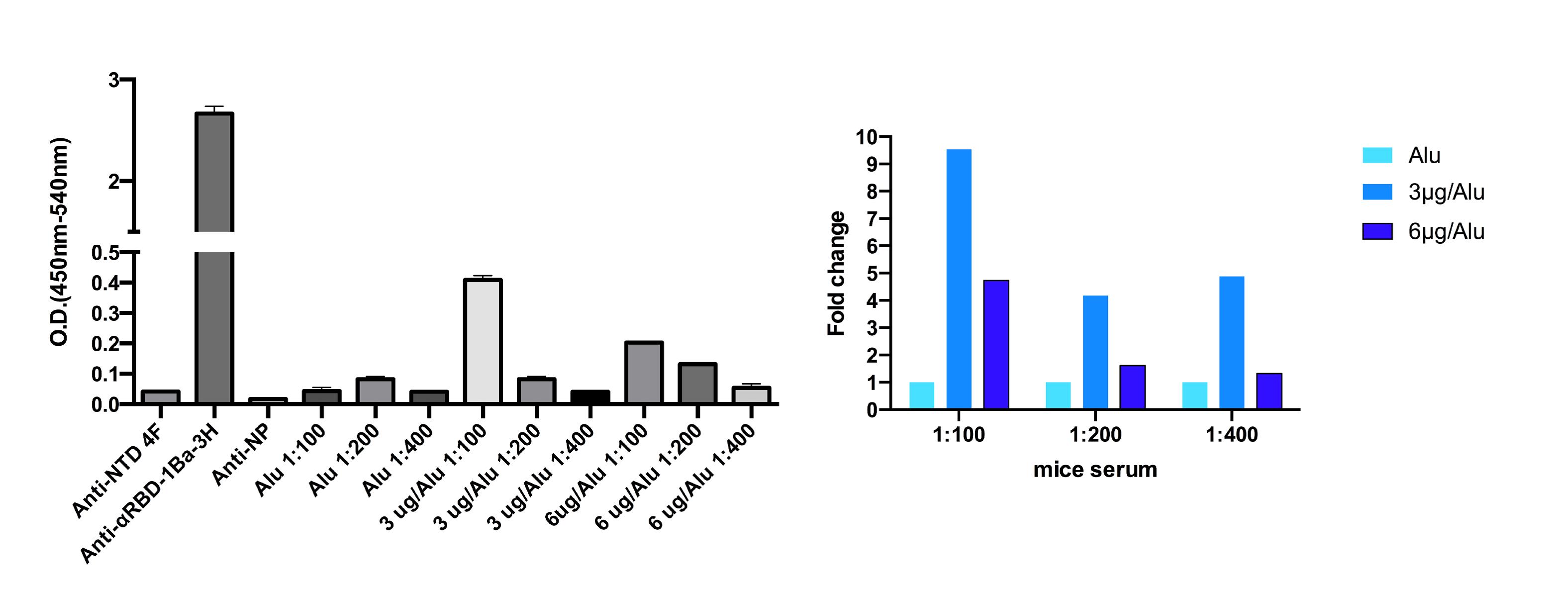
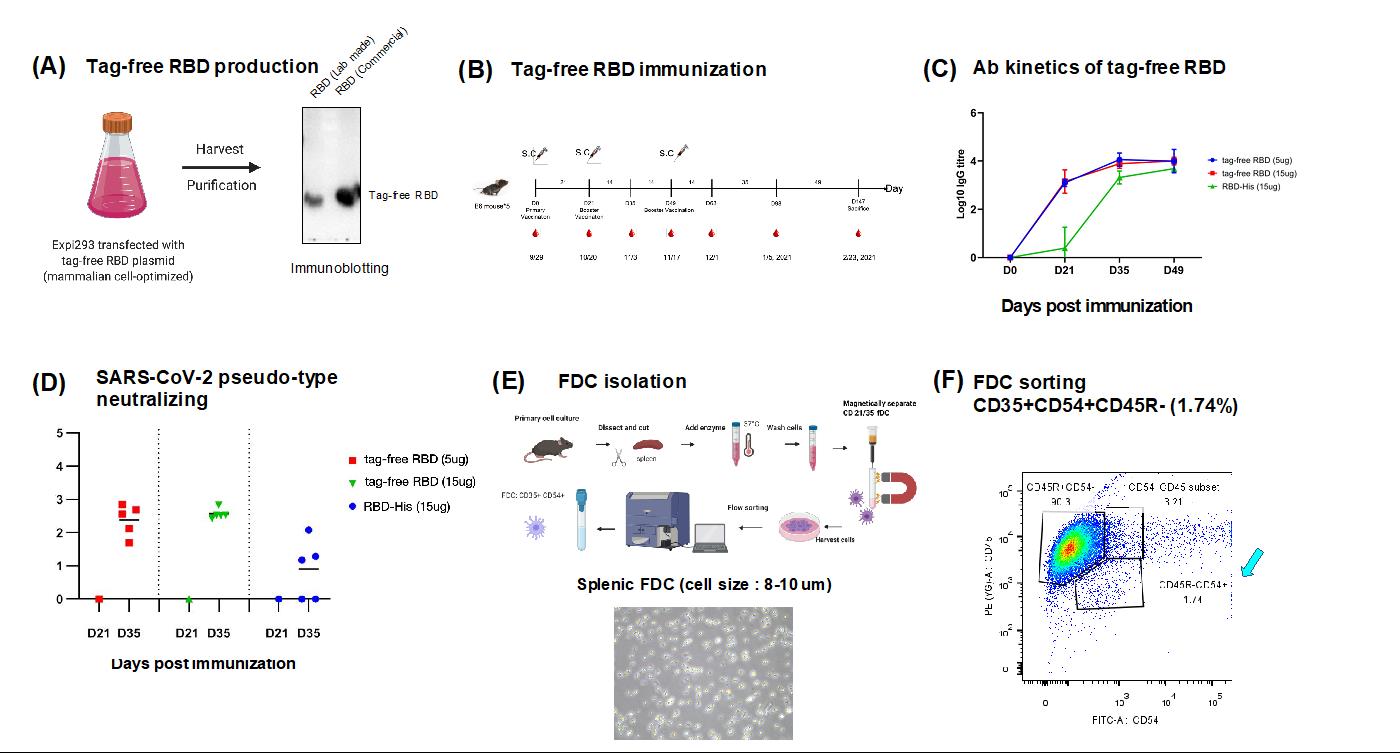
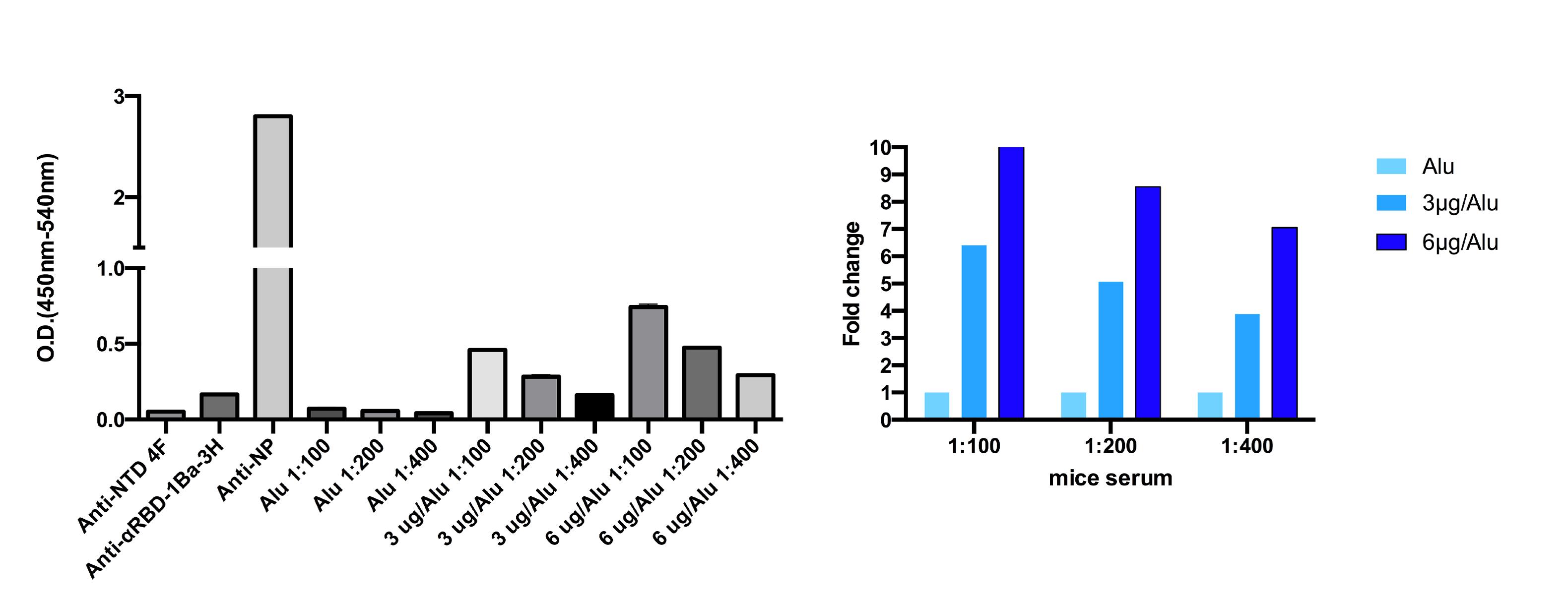 2. 開發基於SARS-CoV-2受體結合區(RBD)的疫苗:
2. 開發基於SARS-CoV-2受體結合區(RBD)的疫苗:
我們已經構建並使用293T細胞系統表達了重組的RBD。每升細胞培養物的產量可以達到20 mg。如表達hACE2的細胞所證實,重組RBD顯示出與人類ACE2良好的結合親和力。透過PNGase F處理後分子量的變化也證明了重組RBD具有適當的糖基化。RBD的抗原性也已經使用人類恢復期血清進行了驗證。
C57BL/6小鼠接種了市售RBD-Fc或實驗室內部生產的RBD加上鋁鹽的混和物,在實驗第35天已接種二次RBD後,抗RBD特異性IgG效價顯著增加,第49天進行額外的免疫進一步提高了第63天的抗RBD IgG效價。
第一次免疫後,RBD-Fc誘導的中和抗體在第21天,效價從1:40到1:160。隨後的加強免疫將第35天和第63天的中和效價分別提高到1:320和1:1280。在對於以RBD免疫的實驗中,在第49天第三次給藥後,顯著的中和抗體效價可以被檢測到,在第63天的效價在1:40至1:2560之間。這些結果表明SARS-CoV-2 的RBD是疫苗開發中有效的候選人。
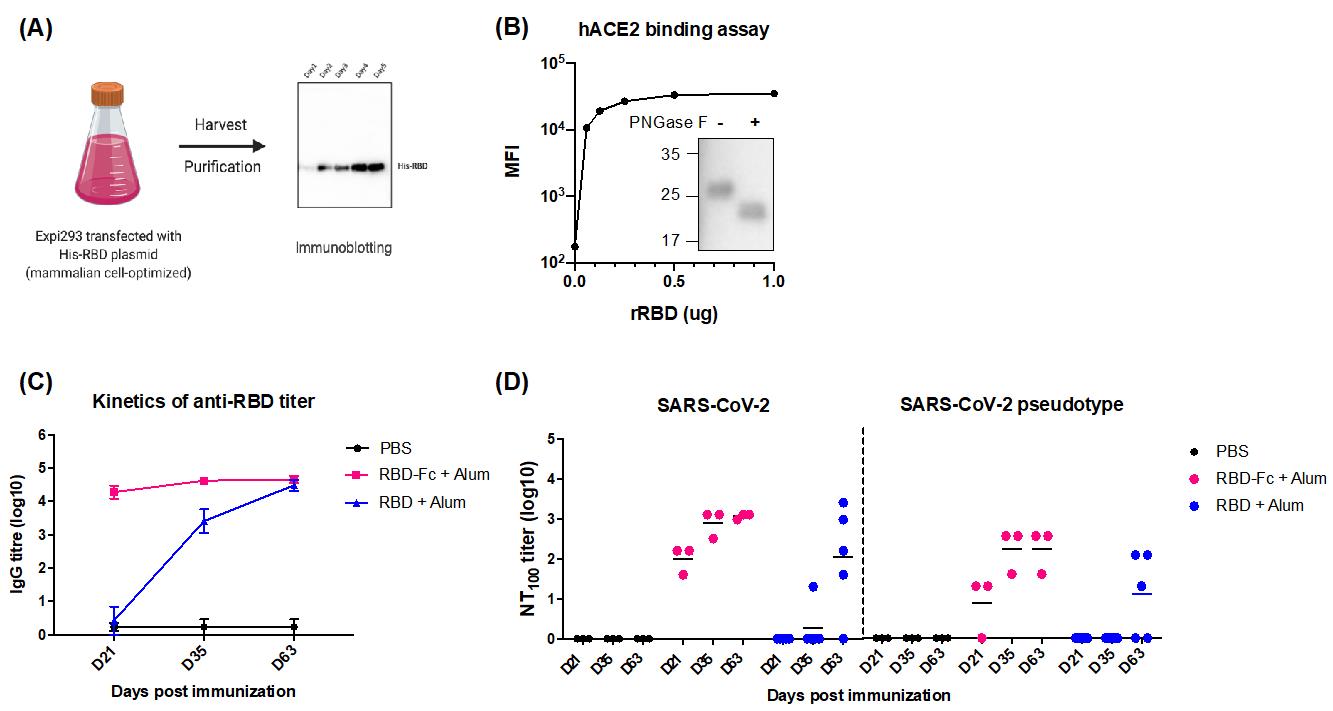
為了進一步增強RBD的免疫特異性,我們表達了無標籤的RBD,並通過離子交換純化了蛋白質。通過皮下注射向小鼠注射無標籤的RBD,並監測免疫反應。結果表明,與His標籤的RBD相比,無標籤的RBD在免疫後的所有時間點都能誘導更高的抗原特異性抗體和中和抗體。
我們並在含血清的試管中收取SPF C57BL/6小鼠脾臟。通過CD21 / 35磁珠放大,並使用流式細胞儀進行分選, CD35 + CD54 + CD45R-的小鼠脾濾泡性樹突狀細胞(FDC)已成功分離和分類。此細胞將用於隨後的細胞凝膠化和噬菌體展示的研究中。
3. 發展使用HBc類病毒顆粒來誘發黏膜性免疫反應的SARS-CoV-2疫苗:
為了評估刺突蛋白上RBD的黏膜免疫原性,在第0、14和28天用5 ug重組大腸桿菌熱不穩定腸毒素B次單元(LTB)或25 µg HBc類病毒顆粒混和10 µg或25 µg RBD免疫5至8週齡的BALB/c小鼠(每組5隻)。並使用ELISA分析了第42天收集的最終血清的RBD特異性IgG反應。
結果表明,與單獨接受25μg RBD或PBS的小鼠相比,接受鼻內免疫HBc或LTB加上25μg RBD混合物的小鼠可產生顯著更高的血清RBD特異性總IgG和肺沖洗液中RBD特異性分泌型IgA。並利用脾細胞對重組RBD體外刺激產生的IFN-γ來評估了保護性的Th1-bias免疫反應。
結果顯示,在接受PBS的小鼠脾細胞中檢測到的IFN-γ低於300μg/ ml。用RBD / HBc免疫的小鼠的脾細胞在RBD刺激後表現出明顯更高的IFN-γ分泌(300-2300μg/ ml,p <0.05)。
1. 與國內疫苗廠簽署產學合作,進行第一期新冠疫苗臨床試驗的人體抗體效價測試。測試結果將有利於國內疫苗的研發及製備,對於 疫情的控制有莫大的助益。
2. 與國內疫苗廠簽署產學合作,進行COVID-19去活化疫苗研究計畫,小規模測試去活化病毒在疫苗廠的純化流程及對小鼠的免疫反 應。
3. 林淑華教授、陳佑宗副教授及游益興博士自行研發人源化之ACE2轉基因小鼠,可幫助國內研究人員或相關產業發展不受限於國外 之專利。
4. 由於傳染病和人畜共通疾病的高患病率,全球疫苗佐劑的市場從2016年的4.67億美金增加到2021年的7.694億美金,各個政府機構 也日益重視對現有或新興疾病的疫苗接種規劃,並且越來越重視疫苗的改進及長效性的疫苗。
由於黏膜疫苗能夠有效地誘導黏膜免疫反應、價格便宜、容易接種、適合大規模疫苗接種等屬性而得到越來越多的重視。而我們的 候選佐劑HBc類病毒顆粒是從B型肝炎病毒(HBV)外殼蛋白自行組裝形成的不具有活性的奈米顆粒,不帶有遺傳物質,所以它們 是不具有感染性且相對安全的候選佐劑。